W branży wyrobów medycznych zgodność z odpowiednimi standardami jest kluczowa dla zapewnienia bezpieczeństwa pacjentów, skuteczności klinicznej oraz utrzymania zgodności z wymaganiami regulacyjnymi na rynkach lokalnych i międzynarodowych. Dobór odpowiednich norm zależy od klasy, rodzaju i przeznaczenia wyrobu.
Wszystkie normy techniczne mające zastosowanie do wyrobów medycznych – w tym standardy zharmonizowane z wymaganiami MDR, FDA CFR czy MDSAP – podlegają okresowym przeglądom i aktualizacjom. Celem tych aktualizacji jest uwzględnianie postępu technologicznego i oczekiwań regulatorów.
Aktualizacja standardów często wynika z:
- postępu technologicznego,
- zmian legislacyjnych,
- zgłaszanych problemów z interpretacją standardów,
- wyników badań nad bezpieczeństwem wyrobów,
- wniosku z prowadzonego systemu nadzoru nad produktem wprowadzonym do obrotu (Medical Devices Vigilance),
- potrzeb doprecyzowania wymagań.
Z punktu widzenia zapewnienia jakości i zarządzania ryzykiem, pominięcie dostosowania do najnowszych wersji standardów może negatywnie wpływać na bezpieczeństwo pacjentów i użytkowników.
Oprócz tego, może prowadzić do poważnych konsekwencji, takich jak:
- cofnięcie certyfikacji,
- opóźnienia we wprowadzaniu wyrobów na rynek,
- zwiększone ryzyko reklamacji,
- konieczność wycofania produktów.
Ze względu na ryzyka regulacyjne oraz konieczność utrzymania zgodności z aktualnymi wymaganiami, wiele organizacji w branży wyrobów medycznych decyduje się na wdrożenie systemowego procesu monitorowania, oceny i aktualizacji stosowanych standardów.
Monitorowanie standardów i identyfikacja zmian
Dobrze zaprojektowany proces zapewnia organizacji szybkie reagowanie na zmiany, planowanie działań adaptacyjnych oraz unikanie ryzyka braku zgodności.
Monitorowanie zmian może być zorganizowane w różnorodny sposób, w zależności od skali działalności organizacji i dostępnych zasobów. W mniejszych firmach może to być jednoosobowa odpowiedzialność specjalisty ds. jakości czy specjalisty ds. regulacji, natomiast w większych korporacjach częstą praktyką jest powołanie zespołu opiekującego się procesem. Specjalista odpowiedzialny za proces musi działać w porozumieniu z ustanowioną w firmie osobą odpowiedzialną za zgodności regulacyjne.
Subskrypcje i członkostwa
Najbardziej bezpośrednim sposobem monitorowania zmian w standardach jest subskrybowanie powiadomień i newsletterów publikowanych przez organizacje normalizacyjne. Międzynarodowe oraz krajowe organizacje, takie jak:
umożliwiają założenie konta użytkownika, zapisanie się do newsletterów tematycznych lub otrzymywanie powiadomień o nowych publikacjach i projektach standardów. Uczestnictwo w komitetach technicznych i grupach roboczych daje dodatkowo dostęp do informacji na wczesnym etapie tworzenia lub rewizji standardów. W ten sposób możliwe jest nie tylko poznanie przyszłych wymagań, ale też wpływanie na ich kształt.
Monitoring regulacyjny
Monitoring regulacyjny to proces polegający na systematycznym śledzeniu zmian w przepisach prawa oraz dokumentach powiązanych, które mają wpływ na obowiązujące standardy. Dla firm działających w sektorze wyrobów medycznych oznacza to konieczność obserwowania wielu źródeł, zarówno międzynarodowych, jak i krajowych. Zmiany legislacyjne mogą bowiem wpływać nie tylko na samą treść standardów, ale również na ich status – np. uznanie danego dokumentu za standard zharmonizowany.
Aby skutecznie zarządzać tym procesem, należy wyznaczyć dedykowaną osobę lub zespół, który będzie odpowiedzialny za śledzenie zmian w przepisach regulacyjnych. Taka osoba powinna regularnie analizować komunikaty publikowane przez instytucje takie jak:
- Komisja Europejska – lista zharmonizowanych standardów
- FDA – Recognized Consensus Standards
- Health Canada – Guidance Documents
- TGA Australia
Dodatkowo przydatne są komercyjne systemy wspomagające monitoring regulacyjny:
- Compliance Navigator (BSI)
- Emergo Regulatory Tracker – RAMS
- Regulatory Affairs Professionals Society – RAPS
Systemy te pozwalają na stworzenie spersonalizowanego panelu informacyjnego, który filtruje standardy zgodnie z wybranymi kategoriami, typami dokumentów czy regionami. Można dzięki nim ustawić alerty mailowe, powiadomienia o rewizjach dokumentów oraz otrzymywać interpretacje i analizy ekspertów. Narzędzia te są szczególnie przydatne dla organizacji o międzynarodowym zasięgu.
Oprócz pasywnego monitorowania źródeł zewnętrznych, warto rozważyć cykliczny, wewnętrzny przegląd stosowanych standardów. W ramach takiego przeglądu:
- aktualizuje się wykaz standardów stosowanych przez organizację,
- weryfikuje się, czy istnieją nowsze wersje dokumentów,
- sprawdza się daty publikacji, terminy wycofania oraz wymagania przejściowe.
Taki przegląd może być połączony z audytem wewnętrznym lub przeglądem systemu zarządzania jakością (QMS).
Wewnętrzne procedura wdrażania standardów
W systemie zarządzania jakością musi znaleźć się procedura lub instrukcja opisująca sposób identyfikacji oraz oceny wpływu nowych wersji standardów. Dokument ten może zawierać:
- definicję odpowiedzialności za monitorowanie,
- ścieżkę eskalacji informacji do kierownictwa,
- obowiązek przeprowadzenia oceny wpływu,
- wymagania dotyczące dokumentacji działań.
Odpowiedzialność co do utrzymywania takiej instrukcji jest zazwyczaj przypisana do specjalisty ds. jakości i specjalisty ds. regulacji. Posiadając instrukcję, należy także zadbać o szkolenia dla nowych pracowników, tak aby byli świadomi roli standardów w procesach firmy oraz wiedzieli, jak identyfikować zmiany i zgłaszać je do odpowiednich osób.
Etapy skutecznego wdrażania nowych wersji standardów
Skuteczne wdrożenie nowej wersji standardu wymaga planowego podejścia, jasnego przydziału ról i odpowiedzialności oraz dokładnej analizy zmian. Proces ten można podzielić na następujące etapy.
1. Ocena wpływu
Każda nowa wersja standardu powinna zostać oceniona pod kątem zmian w stosunku do poprzedniej wersji. Ocena ta powinna być przeprowadzona przez zespół interdyscyplinarny, który uwzględnia zarówno aspekty techniczne, jak i regulacyjne.
Zakres oceny powinien obejmować:
- identyfikację istotnych zmian w wymaganiach,
- ocenę, czy zmiany mają wpływ na projekt, produkcję, testowanie, dokumentację lub system zarządzania jakością,
- ocenę ryzyka związanego z brakiem wdrożenia zmian,
- określenie obowiązujących terminów przejściowych.
Należy sporządzić sprawozdanie lub raport z oceny wpływu, który zawiera podsumowanie zmian, analizę ryzyka, rekomendacje oraz decyzję dotyczącą dalszych działań. Taki dokument musi również zawierać przypisanie odpowiedzialności i wskazanie, które działy muszą podjąć określone działania.
2. Plan wdrożenia
Po ocenie wpływu należy opracować plan wdrożenia nowej wersji standardu. Plan ten powinien zawierać:
- listę działań wymaganych do wdrożenia zmian,
- odpowiedzialnych za realizację,
- terminy wykonania poszczególnych działań,
- sposób weryfikacji skuteczności wdrożenia,
- sposób komunikacji zmian w organizacji.
Plan powinien być zatwierdzony przez kierownictwo i monitorowany pod kątem realizacji. Wdrożenie można rozłożyć na etapy – w pierwszej kolejności zmiany o wysokim priorytecie, a następnie mniej krytyczne elementy. Warto także zaplanować rezerwę czasową na konsultacje z jednostką notyfikowaną, jeśli zmiany wpływają na dokumentację techniczną lub certyfikację.
3. Wdrożenie zmian
Realizacja zaplanowanych działań może obejmować:
- aktualizację procedur i instrukcji,
- szkolenia dla pracowników,
- modyfikację dokumentacji produktu,
- aktualizację zapisów w systemie zarządzania jakością,
- przeprowadzenie audytów wewnętrznych.
Ważne jest, aby wszystkie działania były odpowiednio udokumentowane. Dokumentacja ta będzie później podstawą do wykazania zgodności podczas audytu zewnętrznego lub przeglądu przez jednostkę certyfikującą. Szczególną uwagę należy zwrócić na spójność między różnymi obszarami dokumentacji (np. procedury, instrukcje robocze, formularze).
4. Weryfikacja i utrzymanie zgodności
Po zakończeniu wdrożenia należy zweryfikować, czy wszystkie wymagania nowej wersji standardu zostały spełnione. Może to obejmować:
- przeprowadzenie audytu wewnętrznego,
- przegląd dokumentacji,
- aktualizację deklaracji zgodności,
- monitorowanie działań powdrożeniowych.
Utrzymanie zgodności powinno być elementem ciągłego doskonalenia systemu zarządzania jakością. Wskazane jest prowadzenie działań następczych, takich jak audyty powdrożeniowe czy ankiety wewnętrzne oceniające skuteczność implementacji. Wnioski z tych działań mogą służyć jako podstawa do udoskonalenia przyszłych procesów wdrażania zmian w standardach.
Co zawrzeć w ocenie nowej wersji standardu?
Ocena nowej wersji standardu to kluczowy etap procesu wdrażania, który pozwala określić zakres i charakter wymaganych zmian w systemie zarządzania jakością. Prawidłowo przeprowadzona ocena wpływu pozwala zaplanować działania w sposób adekwatny do potrzeb organizacji oraz zminimalizować ryzyko błędów interpretacyjnych lub wdrożeniowych.
W procesie oceny warto uwzględnić następujące aspekty:
- Zakres zmian: czy nowa wersja standardu wprowadza jedynie zmiany redakcyjne, czy też zawiera istotne zmiany merytoryczne? Należy zidentyfikować nowe wymagania, usunięte zapisy, zmienione definicje i podejścia.
- Wymagania obligatoryjne vs. zalecenia: ważne jest rozróżnienie, które zapisy są obligatoryjne, a które mają charakter zaleceń lub dobrych praktyk – co wpływa na priorytetyzację działań.
- Wpływ na procesy organizacyjne: w jakim stopniu zmiany dotykają poszczególnych procesów – np. projektowania, produkcji, nadzoru nad dostawcami, postmarket surveillance? Czy konieczna będzie zmiana procedur lub instrukcji?
- Wpływ na dokumentację: które dokumenty muszą zostać zmienione lub opracowane od nowa? Czy aktualizacja dokumentacji wymaga zatwierdzenia przez jednostkę notyfikowaną?
- Ryzyko braku zgodności: jakie są potencjalne konsekwencje niepełnej implementacji zmian? Czy istnieje ryzyko niezgodności w kontekście certyfikacji, audytów, zgodności z MDR/IVDR itp.?
- Zasoby i czas: jakie zasoby (personel, budżet, narzędzia) będą potrzebne do przeprowadzenia zmian? Ile czasu realnie potrzeba na ich wdrożenie?
- Szanse na usprawnienia: czy zmiany w standardzie mogą być wykorzystane do optymalizacji procesów, poprawy skuteczności lub jakości, redukcji ryzyk?
Ocena wpływu powinna być przeprowadzana w sposób interdyscyplinarny, z udziałem osoby odpowiedzialnej za zgodność regulacyjną oraz przedstawicieli różnych działów, aby zapewnić pełne zrozumienie konsekwencji zmian. Dobrą praktyką jest tworzenie raportu z oceny wpływu, który dokumentuje ustalenia i rekomendacje.
Dobre praktyki w procesie wdrażania
Choć każde przedsiębiorstwo może wypracować własne metody działania, istnieje kilka uniwersalnych zasad, które sprawdzają się niezależnie od wielkości firmy czy jej specjalizacji w sektorze wyrobów medycznych.
1. Ustanowienie właściciela procesu
W każdej organizacji powinna być jasno określona osoba odpowiedzialna za cały proces wdrażania nowej wersji standardu. Taki właściciel procesu (np. specjalista ds. jakości, kierownik RA/QA lub kierownik projektu) pełni rolę koordynatora, który nadzoruje harmonogram, przypisuje zadania, monitoruje ryzyko i rozwiązuje problemy pojawiające się w trakcie implementacji.
2. Wczesne angażowanie interesariuszy
Dobrą praktyką jest jak najwcześniejsze włączanie w proces wszystkich działów, które mogą być dotknięte zmianami – m.in. działu badań i rozwoju, produkcji, kontroli jakości, marketingu oraz personelu klinicznego. Dzięki temu możliwe jest uzyskanie pełniejszego obrazu skutków zmian oraz wcześniejsze wykrycie ewentualnych barier lub potrzeb szkoleniowych.
3. Analiza luk (ang. gap assessment)
Zanim przystąpi się do implementacji zmian, należy przeprowadzić analizę porównawczą istniejącego systemu zarządzania jakością z nowymi wymaganiami standardu. Analiza ta pozwala na określenie braków oraz ocenę, jak duże zmiany są wymagane. Dokumentacja takiej analizy jest również przydatna jako dowód podczas audytów zewnętrznych.
4. Komunikacja zmian
Regularna i przejrzysta komunikacja jest jednym z kluczowych elementów udanego wdrożenia. Zespół projektowy powinien przygotować jasne komunikaty, w tym streszczenia najważniejszych zmian czy ich wpływ zmian na codzienne obowiązki. Odpowiednia komunikacja zwiększa akceptację zmian i ułatwia ich wdrożenie.
5. Szkolenia dostosowane do ról
Szkolenia powinny być nie tylko obowiązkowe, ale i dostosowane do konkretnego stanowiska. Pracownicy operacyjni powinni otrzymać praktyczne instrukcje dotyczące nowych wymagań, natomiast osoby zarządzające – narzędzia do monitorowania zgodności. Szkolenia powinny kończyć się testem wiedzy lub weryfikacją kompetencji, co stanowi dowód skuteczności procesu.
6. Stopniowe wdrażanie i podejście iteracyjne
Wdrażanie zmian może przebiegać efektywniej, jeśli zostanie rozłożone na etapy, np. w pierwszej kolejności można wdrożyć zmiany w dokumentacji i szkoleniach, a dopiero potem przejść do zmian w procesach technicznych lub systemach informatycznych. Takie podejście pozwala na bieżąco identyfikować przeszkody i elastycznie modyfikować plan.
7. Dokumentowanie całego procesu
Każdy etap wdrożenia należy udokumentować. W skład tej dokumentacji mogą wchodzić:
- plan wdrożenia,
- raport z oceny wpływu,
- harmonogram działań,
- protokoły szkoleń,
- zapisy z przeglądów,
- rejestry zmian w procedurach i instrukcjach.
Kompletna dokumentacja nie tylko potwierdza przejrzystość procesu, ale także chroni organizację przed potencjalnymi zarzutami braku należytej staranności w przypadku audytów.
8. Przegląd powdrożeniowy
Po zakończeniu wdrożenia należyprzeprowadzić formalny przegląd powdrożeniowy, którego celem jest ocena skuteczności podjętych działań. W trakcie przeglądu można ocenić zgodność z założeniami planu, skuteczność szkoleń oraz poziom zaangażowania interesariuszy. Wnioski z przeglądu powinny posłużyć jako baza wiedzy do przyszłych wdrożeń.
Formatka do oceny nowej wersji standardu
W celu usystematyzowania procesu analizy nowo opublikowanych standardów, warto przygotować ustrukturyzowaną formatkę do oceny ich wpływu. Taki dokument wspiera nie tylko spójność podejścia i pełność analizy, ale również stanowi wartość dowodową podczas audytów zewnętrznych. Ułatwia komunikację między działami oraz dokumentuje decyzje i wnioski wynikające z przeglądu zmian.
Formatka ta powinna być wykorzystywana każdorazowo po publikacji nowej wersji standardu istotnego dla działalności firmy. Może być przygotowywana przez osobę odpowiedzialną za system zarządzania jakością, regulatory affairs lub specjalny zespół interdyscyplinarny. Należy ją zatwierdzić na poziomie kierownictwa, a wnioski z oceny powinny stanowić podstawę do utworzenia planu wdrożenia.
Poniżej przedstawię przykładową formatkę, która może być wykorzystana do przeprowadzenia oceny wpływu nowej wersji standardu. Dokument taki może być wypełniany przez zespół projektowy lub pełnomocnika ds. jakości i stanowić podstawę do dalszego planowania wdrożenia.
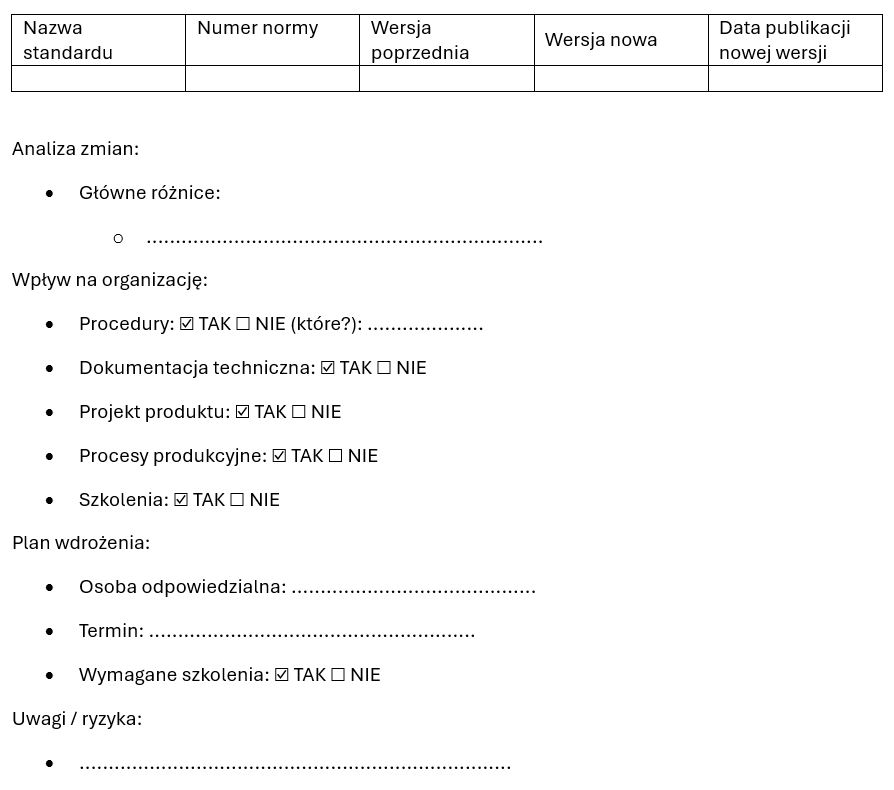

Podsumowanie
Wdrażanie nowych wersji standardów w organizacji medycznej to złożony i wieloetapowy proces, który wymaga systematyczności, interdyscyplinarnego podejścia i strategicznego planowania.
W szczególności, skuteczne wdrożenie wymaga odpowiednio zaplanowanego procesu monitorowania, który pozwoli organizacji szybko reagować na zmiany i zapobiegać niezgodnościom. Ocena wpływu nowej wersji standardu powinna być przeprowadzana metodycznie i dokumentowana, aby stanowić podstawę do dalszych działań wdrożeniowych.
Wdrożenie powinno być realizowane etapowo, przy zaangażowaniu odpowiednich zespołów i uwzględnieniu dostępnych zasobów. Dobre praktyki, takie jak przeprowadzanie szkoleń, aktualizacja dokumentacji, komunikacja między działami czy wykorzystanie szans na optymalizację, znacząco podnoszą skuteczność procesu i jego wartość dodaną.
Warto zatem inwestować w rozwój kompetencji zespołu, systemy monitorowania zmian oraz narzędzia wspierające analizę i wdrażanie nowych wymagań – przekłada się to na jakość wyrobów i bezpieczeństwo pacjentów.

















































Zostaw komentarz